上海艾跃(Active Motif)生物科技有限公司品牌商
9 年
手机商铺
- NaN
- 0.3999999999999999
- 0.3999999999999999
- 2.4
- 2.4
上海艾跃(Active Motif)生物科技有限公司
入驻年限:9 年
- 联系人:
Active Motif
- 所在地区:
上海 闵行区
- 业务范围:
试剂、实验室仪器 / 设备、技术服务、抗体
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
致癌Ras蛋白为什么这么火?多个靶向药接连获批?扒一扒来龙去脉!
4962 人阅读发布时间:2022-07-21 13:26
Ras是一种21kDa的小GTPase蛋白,看似微不足道,但具有非常独特的命运。
Ras首先在逆转录病毒中发现,在逆转录病毒中,Ras被发现与RNA肿瘤病毒的致癌能力有关。
从那时起,Ras的同源物相继在原核生物和真核生物基因组中被发现。
Ras被多种信号通路激活,反过来可以激活许多下游蛋白质和转录因子。
广泛的Ras相互作用组意味着它与几个发育过程以及病理失调有关。
Ras广泛参与癌症的发生,并显示出特定的突变,这些突变通常与不同类型的癌症和临床病理特征相关。
近年来,由于Ras缺乏药物相互作用的结构口袋,大家都认为无法从Ras入手制药。
然而,随着蛋白质家族晶体结构的新发现,科学工作者已经能够构建与Ras蛋白结合的靶向化合物,其中一些甚至对某些突变体具有特异性。
在本文中,我们将向大家讲述Ras蛋白的神奇故事,世界各地的研究人员如何识别该蛋白家族、破译由Ras调节的复杂信号网络、以及它与癌症发展的关系。
Ras历史:从逆转录病毒研究到癌症研究 Ras发现
20世纪60年代人们从啮齿动物、猫、猴子、鸡和火鸡中分离转化逆转录病毒进行研究,从而发现了Ras蛋白。
Harvey鼠肉瘤病毒(1964)和Kirsten鼠肉瘤病毒(1967)在培养基中能快速转化动物细胞,Ras的名字来自其促进大鼠肉瘤(rat sarcoma)的能力,不同的变体以每个发现者的名字命名:H-Ras或Ha-Ras代表Harvey,K-ras或Ki-ras代表Kirsten。
直到1973年,Scolnick等人才假设这些病毒的致癌特性是由于将正常的细胞序列引入它们自己的基因组。
为了证实他们的假设,Scolnick等人在70-80年代领导了广泛、新颖的研究,以确定K-ras和H-ras的细胞起源。
这些基因编码一种21k Da蛋白,能够结合GDP并与质膜相关。
出乎意料的是,他们发现了病毒基因的细胞同源物,这种同源物也与GTP/GDP结合,并且当过度表达时,它会诱导细胞转化。
这些研究成为Ras生化和细胞分析的基础。
不幸的是,这些逆转录病毒最初并没有被认为与癌症有关,因此它们没有得到太多关注。
然而,“活性真核DNA可以转移到哺乳动物细胞中”这一发现被用来开发一项重要技术——磷酸钙转染。
第一个实验是在永生化NIH/3T3细胞系中进行的。
在癌基因逆转录病毒感染后,NIH/3T3显示出生长因子独立性和失去接触抑制,两者都是恶性肿瘤的特征。
这是 “肿瘤基因”特征研究开始的一部分,包括了RAS和RAS突变。
1982年,三个独立的研究小组(Barbacid、Cooper、Weinberg)鉴定出在转染试验中与NIH/3T3转化相关的,与Kirsten和Harvey相同的RAS基因。
同年年底,其他三个研究小组(Wigler、Barbacid、Chang)发表了EJ/T24膀胱癌细胞系中H-Ras激活的分子基础。
出乎意料的是,密码子12中的一个错义突变与H-Ras的组成性激活有关。
同样的突变也在K-Ras中发现,并与肺和结肠肿瘤细胞中的K-Ras激活有关。
1983年,在神经母细胞瘤衍生的DNA中发现了第三种RAS基因,称为N-RAS。
后来,在人类肿瘤组织中发现了密码子12突变,但在正常组织中没有,这一发现证实了Ras突变不仅仅是体外细胞传代的副作用的观点。
认识到一个单一的突变可以导致致癌,这引发了在Ras背景下对癌症分子机制的新的、激烈的研究领域,并为其它Ras突变的发现铺平了道路。
Ras-GTPase蛋白家族
RAS基因在动物界高度保守,但在植物中没有发现。
酿酒酵母(S. cerevisiae)有两种功能冗余的Ras蛋白,Ras1和Ras2,它们与孢子活力有关。
在果蝇中,Dras1和Dras2是RAS同源物,在眼睛发育中发挥作用。
编码秀丽隐杆线虫(C. elegans)LET-60蛋白的RAS基因调节外阴发育。
此外,在网柄菌和斑马鱼中也发现了Ras蛋白。
跨物种的序列同源性和结构分析已比对到RAS GTPase超家族中的5个分支:RAS、Rho、Rab、Arf和Ran。
Ras蛋白包含6条β链和5条α螺旋。
它们拥有一个G结构域和一个C端高变区(HVRs)。
包含switch I、Switch II和P loop序列的结构域负责GTP/GDP绑定。
HVR结构域是翻译后修饰的靶点,包括异丙氨酸化、蛋白质水解和甲基化,介导Ras-质膜结合。
Ras蛋白在严格调控的GTP/GDP循环中,在GDP结合的非活性状态和GTP结合的活性状态之间切换。
包括SOS1在内的鸟嘌呤核苷酸交换因子加速了GDP和GTP之间的转换,以响应上游信号。
相反,GTP酶激活蛋白(GAPS)加速GTP水解。
Ras激活通过与下游效应器结合诱导信号转导。
Ras定位也特别重要,仅在质膜上激活。
这种关联需要Ras翻译后修饰:通过法尼基转移酶(FTase)或香叶基转移酶(GGT)的异戊烯化,通过Ras转换酶(RCE1)切割AAX末端残基,以及通过异丙肾·上·腺·素半胱氨酸羧基甲基转移酶(ICMT)使CAAX box的半胱氨酸甲基化。
Ras一旦到达细胞膜,就会发生寡聚或二聚化。
处于复杂网络中心的Ras
Ras由不同的跨膜受体激活,如细胞因子受体、受体酪氨酸激酶(RTKs)、G蛋白偶联受体(GPCRs)和细胞外基质受体。
它能够将信号转导到包含Ras结合域(RBD)的各种下游效应器,以组织类型和微环境特异性的方式调节转录。
Ras:致癌的主要驱动因素 Ras突变
Ras在19%的癌症中发生突变,这就是为什么它一直是癌症研究领域的热点。
目前公认的是K-Ras是癌症中最常见的突变,其次是N-Ras和H-Ras。
胰腺导管腺癌(PDAC)、肺腺癌(LUAC)、结肠和直肠腺癌的K-Ras突变频率分别为66.1%、16.5%、30.3%和34.4%。
相反,在慢性粒单核细胞白血病(CMML)和急性髓系白血病(AML)等造血肿瘤中,N-Ras突变的发生率分别为13.1%和13.6%。
在黑色素瘤、甲状腺癌和喉癌中,N-Ras突变的发生率分别为18.6%、8.1%和9.7%。
H-Ras突变在人类癌症中非常罕见,仅在唾液腺、口腔和外阴癌中也可以发现。
在RAS基因中已检测到100多个突变,但G12、G13和Q61仍然是K-RAS和N-RAS突变的主要“热点”。
约80%的K-Ras突变位于G12,而60%位于N-Ras的Q61位点。
为什么某些突变在特定条件下更为频繁仍不清楚。
然而,Ras突变赋予肿瘤几个特征:增加增殖能力,促进上皮细胞向间充质细胞转化,以及整体加速肿瘤发展。
更全面的综述可以在《癌症体细胞突变目录》(COSMIC)中找到。
Ras:一种诊断和预后生物标志物
对癌症患者和Ras突变的研究突出了Ras突变与临床病理特征之间的相关性(详情请查看:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8299671/table/Tab1/?report=objectonly)。一个非常典型的例子是大肠癌(CRC)。
携带K-Ras或N-Ras突变的患者总生存率较低。
此外,K-Ras突变与转移扩散到肺部而不是肝脏密切相关。
在黑色素瘤中,N-Ras突变干扰有丝分裂并抑制肿瘤浸润的淋巴细胞。
卵巢癌中K-Ras突变与低分化和高孕酮表达相关。
除了作为一种预后工具外,Ras突变状态还可以指示治疗效果。
在大肠癌转移中,K-Ras突变预测对EGFR抑制剂治疗(例如西妥昔单抗)的耐药性。
Ras突变似乎也可以预测针对免疫检查点阻断(ICB)等负调节因子的治疗效果。
事实上,当肺肉瘤性癌和肺腺癌中有K-Ras相关突变时,作为ICB靶点的蛋白PD-L1具有更好的阻断效率。
Ras:一种药物治疗靶点
鉴于癌症中Ras突变的高频率,开发靶向疗法将是治疗的一个重要进展。
然而,Ras对正常生理过程也很重要。
在这种情况下,药物需要专门针对Ras突变体,以避免有害的副作用。
K-RasG12C靶向治疗
如前所述,由于缺乏潜在的抑制剂结合区及其对GTP/GDP的皮摩尔亲和力,Ras被认为是不可作为靶向药物的切入点的。
然而,2013年,Kevan Shokat的团队成功报告了在GDP结合状态下与K-RasG12C不可逆结合的化合物的开发,阻断了SOS激活和RAF关联。
这些化合物依赖突变半胱氨酸结合,因此不影响野生型蛋白质。
此外,结晶学研究揭示了早期结构中未发现的结合腔的形成。
抑制剂与K-RasG12C的结合破坏了结合囊,随后转移了K-Ras的亲和力,使其偏好GDP而非GTP。
这些发现为针对突变Ras的新的药物发现工作铺平了道路。
安进是第一个成功地将K-Ras抑制剂推向市场的公司。
2021年5月,美国食品和药物管理局批准K-RasG12C抑制剂Lumakras(sotorasib:AMG510)用于先前治疗的表达K-RasG12C突变的转移性非小细胞肺癌患者。
2022年4月,据报道,使用sotorasib治疗的患者两年总生存率为32.5%,比先前的治疗方法有所改善。
sotorasib的长期治疗耐受性良好,毒性轻微且可控。
然而,由于对药物的固有或获得性耐药性,大多数患者没有反应。
来自Mirati的另一种K-RasG12C抑制剂adagrasib:MRTX849可能很快可用于患者。
该抑制剂由AMG510化学衍生而来,结构相似。
2022年2月,美国食品和药物管理局接受了adagrasib的药物申请,用于治疗先前治疗的K-RasG12C非小细胞肺癌患者。
同样的,患者中的耐药性是一个持续性问题。
然而,新的治疗策略正在被尝试,例如将K-RasG12C抑制剂与其他化合物结合以提高疗效。
除上述抑制剂外,安进和Mirati以及其他制药公司(如强生公司、LOXO Oncology、Boehringer Ingelheim、Revolution Medicines、赛诺菲等)正在开发许多其他K-RasG12C抑制剂。
其它突变体
对于其它K-RasG12突变体,如G12D和G12V,需要不同的策略,因为天冬氨酸和缬氨酸的活性低于半胱氨酸。
此外,与K-RasG12C不同,这些突变体在GDP状态下的时间没有那么长。
Shokat在2022年发表的《自然》杂志论文中描述了这些其他突变体如何仍能被非共价配体抑制,并且这种抑制不一定依赖于K-Ras的GDP状态。
这些结果表明由这些其他突变驱动的癌症有了新的治疗机会。
作为K-RasG12D抑制剂之一,Mirati的MRXT1133已经在临床前胰腺癌模型中显示出明显的肿瘤消退。
另一种方法是靶向所有突变并开发“泛Ras”抑制剂。
其中一种化合物,化合物3144对抑制肿瘤增殖和生存非常有效,并且没有显著的不良反应。
它在D38、A59和Y32处结合K-RasG12D、野生型K-Ras、N-Ras和H-Ras。
最后,蛋白质水解靶向嵌合体(PROTACs)是一种能够去除特定不需要的蛋白质的小分子,正在被探索作为阻止突变Ras的方法。
PROTACs利用细胞的泛素-蛋白酶体系统(UPS),将目标蛋白和E3连接酶结合在一起,使其能够泛素化和降解。
其中一种是LC-2,该化合物能够选择性诱导K-RasG12C蛋白质降解。
癌症疫苗
该方法旨在诱导针对特定Ras蛋白突变体的免疫反应。
来自突变Ras蛋白的多肽与重组GM-CSF一起注射到患者体内,以激活树突状细胞并增强T细胞对这些特异性突变的反应。
Targovax的治疗性抗癌疫苗TG01目前正在测试胰腺癌。
在PDAC患者中注射TG01显示免疫应答和总生存率增加。
另一种药物TG02正在大肠癌患者中测试。
由Moderna开发的mRNA疫苗mRNA-5671也在临床试验中。
它编码K-Ras突变,并在脂质纳米粒中形成。
它作为单一药物或与彭布罗利珠单抗(pembrolizumab)联合使用。
间接法-核苷酸交换抑制剂
GTPase活性对Ras功能至关重要。
因此,抑制GDP-GTP交换也可以阻断Ras活性。
SOS蛋白是鸟苷核苷酸交换因子(GEF),可增加Ras 蛋白的GDP和GTP的交换率。
因此,另一种方法是开发直接与SOS而不是Ras结合的小分子。
其中包括BAY-293,它抑制Ras-SOS1相互作用。
单独使用时,它对K-Ras突变蛋白的生理作用较弱。
然而,与K-RasG12C抑制剂ARS-853结合,BAY-293显示出协同生长抑制作用,表明这种小分子联合使用使用时可以进行有效治疗。
另一种化合物BI-1701963正在单独或与曲美替尼(MEK抑制剂)联合用于实体瘤和Ras突变患者的试验。
SHP2抑制剂
SHP2是另一种促进Ras核苷酸交换的蛋白质。
靶向SHP2的目标与SOS抑制剂相同:抑制核苷酸交换,从而抑制Ras GTPase活性。
Revolution Medicines和赛诺菲正在联合开发一种名为RMC-4630的化合物,这是一种在多队列1/2期临床项目中有效的SHP2抑制剂。
RMC-4630目前正在进行单药治疗和与comibetinib联合治疗的试验。
Ras加工抑制剂
该策略旨在防止Ras定位于质膜。
Ras在附着到膜之前经历了几个翻译后修饰步骤,包括异·戊·二·烯化。
法尼基转移酶(FTase)是一种促进Ras异·戊·二·烯化的酶。
虽然在K-和N-Ras中有其他的异·戊·二·烯化方法,但H-Ras只能通过FTase进行异·戊·二·烯化。
因此FTase抑制剂如替吡法尼正在被研究用于治疗涉及H-Ras突变的癌症。
ICMT是另一种参与Ras翻译后修饰的酶从而帮助Ras定位于质膜。
ICMT抑制剂cysmethynil可减缓Ras突变细胞的增殖。
另一种ICMT抑制剂UCM-1336在所有四种亚型中阻止Ras膜结合,无论是哪一种突变都能减少细胞增殖。
这些酶都还没有进入临床试验,因为这些酶也会作用于其他底物,阻断它们的作用可能会导致重要的脱靶效应。
总结
Ras家族是普遍存在于多个物种的几个关键生理过程的中心,在肿瘤发生中起着重要作用,包括CRC、NSCLCC和PDAC。
它处于一个复杂网络的中心,调控着不同的转录程序。
关于Ras过去已经完成了大量工作,今天解读Ras功能的故事还在继续,未来将继续寻求对Ras突变的理解,以作为诊断和预后工具。
现在Ras突变被许多文献提及,并被用作诊断和预后工具。
Ras突变也能够预测某些治疗的效率。
所有这些特性使科学家们更接近于新的靶向Ras蛋白及其突变体以及表征Ras活性的方法。
目前正在进行的几项临床试验已经取得了令人鼓舞的临床前结果。
Ras突变体能够有效地靶向,这一特点为精准医疗铺平了道路。
那么如何快速测定Ras蛋白的活性呢?
试试我们Active Motif的RAS GTPase Chemi ELISA试剂盒吧——
如何快速测定RAS蛋白的活性?
Active Motif近年来基于ELISA实验原理开发出了RAS活性的快速检验试剂盒Ras GTPase Chemi ELISA试剂盒(货号52097),此试剂盒可用于检测和定量细胞或组织提取物中Ras-GTPase的活性,帮助研究者监测活化RAS蛋白水平、研究RAS活化信号通路、检测致癌Ras蛋白、评估可能的治疗化合物。
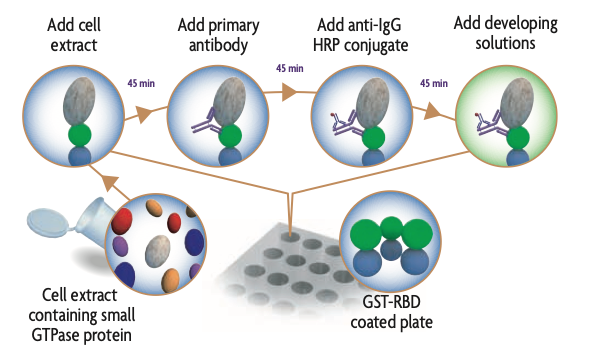
RAS GTPase Chemi ELISA的优势:
-
更高的灵敏度,样本需求量只是pull-down、westerns的5%。
-
更好的结果,定量的读数更好的比较样本间的差异。
-
更省力的实验过程,不需要繁琐的实验步骤,也不需要制胶跑胶。
-
更快得到实验结果,可在5h左右便得到准确的活性结果。
-
适用于多种样本,可以是细胞,组织,也可以是重组蛋白。
-
实验结果可靠,已有15篇发表文献使用了该试剂盒。
如果您有任何疑问,
欢迎联系021-20926090,
18521362870。